Białka błonowe
Białka błonowe – białka związane ze strukturą błony biologicznej.
W błonach tych białka pełnią rozliczne funkcje niezbędne dla prawidłowego funkcjonowania komórki. Występują, między innymi, w roli:
- receptorów – białek przekazujących sygnały między wewnętrznym a zewnętrznym środowiskiem komórki
- enzymów błonowych – białek katalizujących reakcje (głównie oksydoreduktazy, transferazy lub hydrolazy), na przykład kompleksy białkowe syntetyzujące celulozę w komórkach roślinnych
- białek adhezyjnych – uczestniczących w przyleganiu komórek do siebie oraz odpowiedzi immunologicznej
- białek transportowych – służących do transportu jonów i innych cząsteczek chemicznych; są to na przykład kanały błonowe, przenośniki (odpowiadające za transport aktywny), pompy błonowe (np. pompa sodowo-potasowa).
Podział białek błonowych

1. Białko przezbłonowe
2. Białko monowarstwy zewnętrznej
3. Białko monowarstwy wewnętrznej
4. Białko wewnętrzne błony
Niebieskie – białka powierzchniowe
Białka integralne
Białek integralnych nie można łatwo oddzielić od błony (na przykład za pomocą roztworów soli) ze względu na wiązania hydrofobowe z elementami dwuwarstwy lipidowej. Ta klasa białek jest zakotwiczona w błonie motywem białkowym. Do ich ekstrahowania należy używać detergentów. Integralne białka błonowe dzieli się na:
- białka przezbłonowe (transmembranowe), które przebijają całą grubość dwuwarstwy. Białka przezbłonowe można z kolei podzielić na białka jednokrotnie (białka monotopowe) lub wielokrotnie (białka politopowe) perforujące błonę.
- białka nieprzebijające błony, które dzielą się na białka listka (monowarstwy) wewnętrznego i zewnętrznego. Swoistą podgrupą białek nieprzebijających są białka wewnętrzne błony, ulokowane pomiędzy dwoma jej monowarstwami, w jej części hydrofobowej.
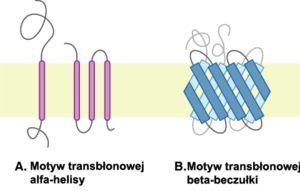
Na szczególną uwagę zasługują sposoby kotwiczenia białek integralnych w dwuwarstwie. Silnie hydrofobowy charakter części lipidowej błony wymusza specyficzną budowę białek: strukturę α helisy lub beczułki beta. Struktury te wymuszają skierowanie polarnych łańcuchów bocznych aminokwasów danego białka do wnętrza struktury, co najczęściej daje efekt polarnego kanału pozwalającego na przepływ odpowiednich polarnych cząsteczek.
Białka powierzchniowe
Białka powierzchniowe łatwo można oddzielić od błony za pomocą roztworów soli. Nie perforują one żadnej z monowarstw błony, a z błoną związane są za pomocą słabych oddziaływań molekularnych, głównie wiązań jonowych, wodorowych i sił van der Waalsa. Oddziałują w ten sposób z samą błoną lub z białkami integralnymi. Te białka mają zwykle duże fragmenty polarne i łączą się z fosfolipidami błony wiązaniami jonowymi.

Białka zakotwiczone
Te białka utrzymywane są w pobliżu błony za pomocą niebiałkowego (lipidowego) elementu zakotwiczonego w błonie. Zależnie od białka można je izolować z błony tylko za pomocą detergentów lub roztworów soli. Białka zakotwiczone zostają wyposażone w motyw kotwiczący na drodze modyfikacji potranslacyjnej. Wyróżnia się następujące modyfikacje białek zakotwiczonych:
- mirystoilacja przy końcu N
- palmitylacja reszt cysteiny
- farnezylacja przy końcu C
- geranylogeranylacja przy końcu C
- glikozylofosfatydyloinozytol na końcu C (motyw cukrowo-lipidowy)
- stearylacja
- oleinacja
- arachidonacja.
W niektórych klasyfikacjach białka zakotwiczone uznaje się za białka integralne błony.
Prawdopodobnie aż 30% białek kodowanych w ludzkim genomie stanowią białka błonowe[1][2][3].
Linki zewnętrzne
- Wyliczone pozycje przestrzenne białek błonowych (ang.)
Przypisy
- ↑ Biochim. Biophys. Acta 1565 (2002) 143 (Editorial)
- ↑ J.-L. Rigaud Membrane proteins functional and structrural studies using reconstituted proteoliposomes and 2-D crystals Brazilian J. of Med. and Biol. Resarch 35 (2002) 753-766
- ↑ J.U. Bowie Stabilizing membrane proteins Curr. Opin. in Struct. Biol. 11 (2001) 397-402








