Lista stopni utlenienia pierwiastków chemicznych
Na liście znajdują się wszystkie znane stopnie utlenienia pierwiastków chemicznych (bez uwzględnienia wartości niecałkowitych). Najpowszechniej występujące stopnie zostały pogrubione. Stopień utlenienia 0, występujący u wszystkich pierwiastków, oznaczony jest symbolem danego pierwiastka w kolumnie. Układ tabeli, ukazujący prawo okresowości, został stworzony przez Mendelejewa w 1889 roku.
| −I | H | I | |||||||||||
| He | |||||||||||||
| Li | I | ||||||||||||
| Be | II | ||||||||||||
| B | I | II | III | ||||||||||
| −IV | −III | −II | −I | C | I | II | III | IV | |||||
| −III | −II | −I | N | I | II | III | IV | V | |||||
| −II | −I | O | I | II | |||||||||
| −I | F | ||||||||||||
| Ne | |||||||||||||
| −I | Na | I | |||||||||||
| Mg | I | II | |||||||||||
| Al | I | III | |||||||||||
| −IV | −III | −II | −I | Si | I | II | III | IV | |||||
| −III | −II | −I | P | I | II | III | IV | V | |||||
| −II | −I | S | I | II | III | IV | V | VI | |||||
| −I | Cl | I | II | III | IV | V | VI | VII | |||||
| Ar | |||||||||||||
| K | I | ||||||||||||
| Ca | II | ||||||||||||
| Sc | I | II | III | ||||||||||
| −I | Ti | II | III | IV | |||||||||
| −I | V | I | II | III | IV | V | |||||||
| −II | −I | Cr | I | II | III | IV | V | VI | |||||
| −III | −II | −I | Mn | I | II | III | IV | V | VI | VII | |||
| −II | −I | Fe | I | II | III | IV | V | VI | |||||
| −I | Co | I | II | III | IV | V | |||||||
| −I | Ni | I | II | III | IV | ||||||||
| Cu | I | II | III | IV | |||||||||
| Zn | II | ||||||||||||
| Ga | I | II | III | ||||||||||
| −IV | Ge | I | II | III | IV | ||||||||
| −III | As | II | III | V | |||||||||
| −II | Se | II | IV | VI | |||||||||
| −I | Br | I | III | IV | V | VII | |||||||
| Kr | II | ||||||||||||
| Rb | I | ||||||||||||
| Sr | II | ||||||||||||
| Y | I | II | III | ||||||||||
| Zr | I | II | III | IV | |||||||||
| −I | Nb | II | III | IV | V | ||||||||
| −II | −I | Mo | I | II | III | IV | V | VI | |||||
| −III | −I | Tc | I | II | III | IV | V | VI | VII | ||||
| −II | Ru | I | II | III | IV | V | VI | VII | VIII | ||||
| −I | Rh | I | II | III | IV | V | VI | ||||||
| Pd | II | IV | |||||||||||
| Ag | I | II | III | ||||||||||
| Cd | II | ||||||||||||
| In | I | II | III | ||||||||||
| −IV | Sn | II | IV | ||||||||||
| −III | Sb | III | V | ||||||||||
| −II | Te | II | IV | V | VI | ||||||||
| −I | I | I | III | V | VII | ||||||||
| Xe | II | IV | VI | VIII | |||||||||
| Cs | I | ||||||||||||
| Ba | II | ||||||||||||
| La | II | III | |||||||||||
| Ce | II | III | IV | ||||||||||
| Pr | II | III | IV | ||||||||||
| Nd | II | III | |||||||||||
| Pm | III | ||||||||||||
| Sm | II | III | |||||||||||
| Eu | II | III | |||||||||||
| Gd | I | II | III | ||||||||||
| Tb | I | III | IV | ||||||||||
| Dy | II | III | |||||||||||
| Ho | III | ||||||||||||
| Er | III | ||||||||||||
| Tm | II | III | |||||||||||
| Yb | II | III | |||||||||||
| Lu | III | ||||||||||||
| Hf | II | III | IV | ||||||||||
| −I | Ta | II | III | IV | V | ||||||||
| −II | −I | W | I | II | III | IV | V | VI | |||||
| −III | −I | Re | I | II | III | IV | V | VI | VII | ||||
| −II | −I | Os | I | II | III | IV | V | VI | VII | VIII | |||
| −III | −I | Ir | I | II | III | IV | V | VI | |||||
| Pt | II | IV | V | VI | |||||||||
| −I | Au | I | II | III | V | ||||||||
| Hg | I | II | IV | [a] | |||||||||
| Tl | I | III | |||||||||||
| −IV | Pb | II | IV | ||||||||||
| −III | Bi | III | V | ||||||||||
| −II | Po | II | IV | VI | |||||||||
| −I | At | I | III | V | |||||||||
| Rn | II | ||||||||||||
| Fr | I | ||||||||||||
| Ra | II | ||||||||||||
| Ac | III | ||||||||||||
| Th | II | III | IV | ||||||||||
| Pa | III | IV | V | ||||||||||
| U | III | IV | V | VI | |||||||||
| Np | III | IV | V | VI | VII | ||||||||
| Pu | III | IV | V | VI | VII | ||||||||
| Am | II | III | IV | V | VI | ||||||||
| Cm | III | IV | |||||||||||
| Bk | III | IV | |||||||||||
| Cf | II | III | IV | ||||||||||
| Es | II | III | |||||||||||
| Fm | II | III | |||||||||||
| Md | II | III | |||||||||||
| No | II | III | |||||||||||
| Lr | III | ||||||||||||
| Rf | IV | ||||||||||||
| Db | V | ||||||||||||
| Sg | VI | ||||||||||||
| Bh | VII | ||||||||||||
| Hs | VIII |
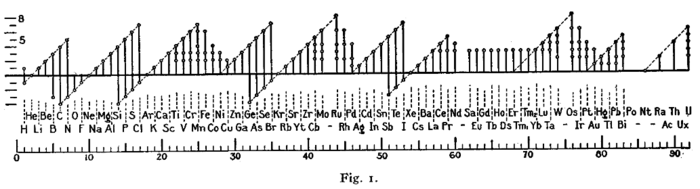
Schemat o podobnym układzie został użyty przez Irvinga Langmuira w 1919 roku w jednej z pierwszych prac o regule oktetu[1]:
Uwagi
- ↑ Hg4+ występuje we fluorku rtęci(IV).
Przypisy
- ↑ Langmuir, Irving. The arrangement of electrons in atoms and molecules. „Journal of the American Chemical Society”. 41 (6), s. 868-934, 1919. DOI: 10.1021/ja02227a002.