Reakcja Chana-Lama
Reakcja Chana-Lama (reakcja Chana-Evansa-Lama, CEL) – reakcja sprzęgania aromatycznego kwasu boronowego (lub jego estrów) z alkoholem lub aminą[1][2], prowadząca do, odpowiednio, aminy aromatycznej lub eteru aromatycznego. Sprzęganie katalizowane jest przez związki miedzi. Może być przeprowadzane w obecności powietrza w temperaturze pokojowej. Reakcja ta w szczególnych przypadkach może być stosowana jako alternatywa dla popularniejszego sprzęgania Buchwalda-Hartwiga[3].
Historia
Reakcja została opisana w 1998 r., w niemal tym samym czasie, niezależnie przez zespoły Dominica Chana[4][5], Davida Evansa[6] i Patrick Lama[7][8].
Przykład
Poniżej przedstawiono przykład reakcji Chana-Lama wykorzystywanej do syntezy złożonych związków aktywnych biologicznie[9].
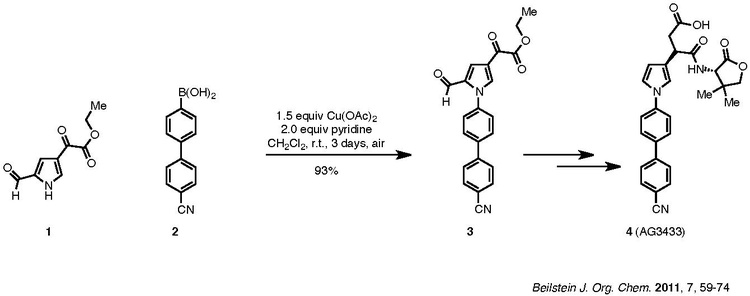
Reaction example of Chan–Lam coupling
Podstawiony pirol (1) sprzęgany jest z aromatycznym kwasem boranowym (2), w wyniku czego powstaje trzeciorzędowa amina (3), która w kolejnych etapach przekształcana jest do docelowego związku (4), silnego inhibitora metaloproteinazy macierzy pozakomórkowej. Sprzęganie CEL prowadzono w temperaturze pokojowej z dostępem powietrza, uzyskując bardzo dobrą wydajność – ponad 90%, jednak czas reakcji wynosił aż 3 dni[9].
Przypisy
- ↑ A. SivaA.S. Reddy A. SivaA.S. i inni, Copper(II)-catalyzed Chan–Lam cross-coupling: chemoselective N-arylation of aminophenols, „Organic & Biomolecular Chemistry”, 15 (4), 2017, s. 801–806, DOI: 10.1039/C6OB02444K (ang.).
- ↑ Julien C.J.C. Vantourout Julien C.J.C. i inni, Chan–Evans–Lam Amination of Boronic Acid Pinacol (BPin) Esters: Overcoming the Aryl Amine Problem, „Journal of Organic Chemistry”, 81 (9), 2016, s. 3942–3950, DOI: 10.1021/acs.joc.6b00466 (ang.).
- ↑ LiliangL. Huang LiliangL., ChengxiangCh. He ChengxiangCh., ZhihuaZ. Sun ZhihuaZ., Application of Chan-Lam cross coupling for the synthesis of N-heterocyclic carbene precursors bearing strong electron donating or withdrawing groups, „Scientific Reports”, 5 (1), 2015, art. nr 12431, DOI: 10.1038/srep12431 (ang.).
- ↑ Dominic M.T.D.M.T. Chan Dominic M.T.D.M.T. i inni, New N- and O-arylations with phenylboronic acids and cupric acetate, „Tetrahedron Letters”, 39 (19), 1998, s. 2933–2936, DOI: 10.1016/S0040-4039(98)00503-6 (ang.).
- ↑ Dominic M.T.D.M.T. Chan Dominic M.T.D.M.T. i inni, Copper promoted C−N and C−O bond cross-coupling with phenyl and pyridylboronates, „Tetrahedron Letters”, 44 (19), 2003, s. 3863–3865, DOI: 10.1016/S0040-4039(03)00739-1 (ang.).
- ↑ David A.D.A. Evans David A.D.A., Jeffrey L.J.L. Katz Jeffrey L.J.L., Theodore R.T.R. West Theodore R.T.R., Synthesis of diaryl ethers through the copper-promoted arylation of phenols with arylboronic acids. An expedient synthesis of thyroxine, „Tetrahedron Letters”, 39 (19), 1998, s. 2937–2940, DOI: 10.1016/S0040-4039(98)00502-4 (ang.).
- ↑ Patrick Y.S.P.Y.S. Lam Patrick Y.S.P.Y.S. i inni, New aryl/heteroaryl C−N bond cross-coupling reactions via arylboronic acid/cupric acetate arylation, „Tetrahedron Letters”, 39 (19), 1998, s. 2941–2944, DOI: 10.1016/S0040-4039(98)00504-8 (ang.).
- ↑ Patrick Y.SP.Y.S. Lam Patrick Y.SP.Y.S. i inni, Copper-promoted/catalyzed C−N and C−O bond cross-coupling with vinylboronic acid and its utilities, „Tetrahedron Letters”, 44 (26), 2003, s. 4927–4931, DOI: 10.1016/S0040-4039(03)01037-2 (ang.).
- ↑ a b CarolinC. Fischer CarolinC., BurkhardB. Koenig BurkhardB., Palladium- and copper-mediated N-aryl bond formation reactions for the synthesis of biological active compounds, „Beilstein Journal of Organic Chemistry”, 7, 2011, s. 59–74, DOI: 10.3762/bjoc.7.10, PMID: 21286396, PMCID: PMC3029007 (ang.).










