Reagente de Petasis
| Reagente de Petasis Alerta sobre risco à saúde | |
|---|---|
 | |
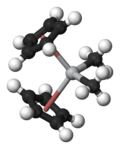 | |
| Nome IUPAC | bi(η5-ciclopentadienil)dimetiltitânio |
| Outros nomes | dimetil-titanoceno |
| Identificadores | |
| Número CAS | 1271-66-5 |
| SMILES |
|
| Propriedades | |
| Fórmula molecular | C12H16Ti |
| Massa molar | 208.13 g/mol |
| Riscos associados | |
| Principais riscos associados | Irritante, incompatível com água e outros agentes oxidantes |
| Página de dados suplementares | |
| Estrutura e propriedades | n, εr, etc. |
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas |
| Dados espectrais | UV, IV, RMN, EM |
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |
O reagente de Petasis (não confundir com a reação de Petasis) é o dimetil-titanoceno,[1] Cp2TiMe2, facilmente preparado pela reação de cloreto de metil-magnésio[2] ou metil-lítio[3] com dicloreto de titanoceno:
- Cp2TiCl2 + 2 "Me−" → Cp2TiMe2 + 2 Cl−
É usado para transformar grupos carbonila em alcenos terminais, tal como o reagente de Tebbe ou a reação de Wittig. Diferentemente da reação de Wittig, o reagente de Petasis pode reagir com uma larga faixa de carbonilas, incluindo aldeídos, cetonas e ésteres.[4] O reagente de Petasis é também mais estável ao ar do que o reagente de Tebbe, e pode ser isolado como sólido puro, ou usado diretamente como solução em tolueno-THF.
O reagente de olefinação ativa, Cp2TiCH2, é preparado pelo aquecimento do reagente de Petasis em tolueno ou THF a 60 °C.
O mecanismo de reação é muito similar ao do reagente de Tebbe, levando primeiro a um carbeno de titânio que forma um oxatitanociclo e então libera o alceno terminal.[5]
Referências
- ↑ N. A. Petasis and E. I. Bzowej (1990). «Titanium-mediated carbonyl olefinations. 1. Methylenations of carbonyl compounds with dimethyltitanocene». J. Am. Chem. Soc. 112 (17): 6392–6394. doi:10.1021/ja00173a035
- ↑ Payack, J. F.; Hughes, D. L.; Cai, D.; Cottrell, I. F.; Verhoeven, T. R. (2002). «Dimethyltitanocene». Org. Synth. 79. 19 páginas !CS1 manut: Nomes múltiplos: lista de autores (link)
- ↑ Claus, K.; Bestian, H. (1962). «Über die Einwirkung von Wasserstoff auf einige metallorganische Verbindungen und Komplexe». Justus Liebigs Ann. Chem. 654. 8 páginas. doi:10.1002/jlac.19626540103 !CS1 manut: Nomes múltiplos: lista de autores (link)
- ↑ Hartley, R. C.; Li, J.; Main, C. A.; McKiernan, G. J. (2007). «Titanium carbenoid reagents for converting carbonyl groups into alkenes». Tetrahedron. 63: 4825–4864. doi:10.1016/j.tet.2007.03.015 !CS1 manut: Nomes múltiplos: lista de autores (link)
- ↑ Meurer, Eduardo Cesar; Santos, Leonardo Silva; Pilli, Ronaldo Aloise; Eberlin, Marcos N. (2003). «Probing the Mechanism of the Petasis Olefination Reaction by Atmospheric Pressure Chemical Ionization Mass and Tandem Mass Spectrometry». Organic Letters. 5. 1391 páginas. doi:10.1021/ol027439b











