Aldolna kondenzacija
Aldolna kondenzacija je organska reakcija u kojoj enol ili enolatni jon reaguje sa karbonilnim jedinjenjem da formira β-hidroksialdehid ili β-hidroksiketon, čemu sledi dehidracija koja daje konjugovani enon.[1][2]

Aldolne kondenzacije su važne u organskoj sintezi. One su dobar način formiranja ugljenik–ugljenik veza. Reakciona sekvenca Robinsonove anulacije sadrži aldolnu kondenzaciju. Vieland-Miešerov ketonski proizvod je važan početni materijal za mnoge organske sinteze.[3][4][5] Aldolna kondenzacija u svojoj uobičajenoj formi, obuhvata nukleofilnu adiciju ketonskog enolata na aldehid da bi se formirao β-hidroksi keton, ili "aldol" (aldehid + alkohol), koji je strukturna jedinica nađena u mnogim prirodnim molekulima i lekovima.[6][7][8]
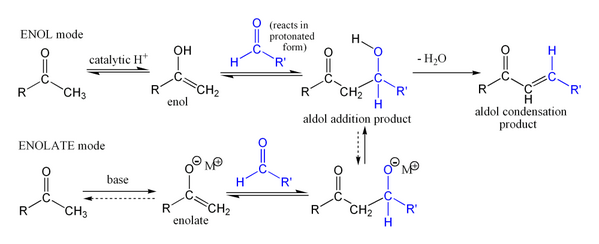
Ime aldolna kondenzacija se takođe često koristi, posebno u biohemiji, za imenovanje aldolne reakcije katalizovane aldolazama. Međutim, aldolna reakcija nije formalno reakcija kondenzacije, jer ne obuhvata gubitak malog molekula.
Reakcije između ketona i aldehida (ukrštena aldolna kondenuacija) ili između dva aldehida su takođe poznate pod imenom Claisen-Schmidt kondenuacija.[9][10][2]
Mehanizam
Prvi deo ove reakcije je aldolna reakcija. Drugi deo je dehidracija — reakcija eliminacije. Dehidracija može da bude praćena dekarboksilacijom kad je prisutna aktivirana karboksilna grupa. Proizvod aldolne adicije može da bude dehidriran putem dva mehanizma: jakom bazom kao što je kalijum t-butoksid, kalijum hidroksid ili natrijum hidrid u enolatu ,[11], ili putem kiselinom katalizovanog enolnog mehanizma.
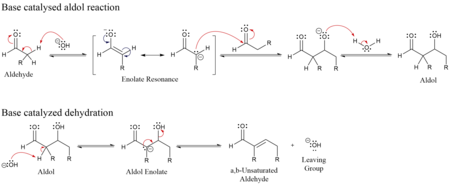 :
:
 |  |
| animation, base catalyzed | animation, acid catalyzed |
Reference
- ↑ Clayden Jonathan, Nick Greeves, Stuart Warren, Peter Wothers (2001). Organic chemistry. Oxford, Oxfordshire: Oxford University Press. ISBN 0-19-850346-6.
- ↑ 2,0 2,1 Smith, Michael B.; March, Jerry (2007). Advanced Organic Chemistry: Reactions, Mechanisms, and Structure (6th izd.). New York: Wiley-Interscience. ISBN 0-471-72091-7.
- ↑ Wade, L. G. (6th ed. 2005). Organic Chemistry. Upper Saddle River, New Jersey: Prentice Hall. str. 1056–1066. ISBN 0132367319.
- ↑ Smith, M. B.; March, J. (5th ed. 2001). Advanced Organic Chemistry. New York: Wiley Interscience. str. 1218–1223. ISBN 0-471-58589-0.
- ↑ Mahrwald, R. (2004). Modern Aldol Reactions, Volumes 1 and 2. Weinheim, Germany: Wiley-VCH Verlag GmbH & Co. KGaA. str. 1218–1223. ISBN 3-527-30714-1.
- ↑ Heathcock, C. H. (1991). Comp. Org. Syn.. Oxford: Pergamon. str. 133–179. ISBN 0-08-040593-2.
- ↑ Mukaiyama T. (1982). „The Directed Aldol Reaction”. Org. React. 28: 203–331. DOI:10.1002/0471264180.or028.03.
- ↑ Paterson, I. (1988). „New Asymmetric Aldol Methodology Using Boron Enolates”. Chem. Ind. 12: 390–394.
- ↑ L. Claisen and A. Claparede (1881). „Condensationen von Ketonen mit Aldehyden”. Berichte der Deutschen chemischen Gesellschaft 14 (1): 2460–2468. DOI:10.1002/cber.188101402192.
- ↑ J. G. Schmidt (1881). „Ueber die Einwirkung von Aceton auf Furfurol und auf Bittermandelöl in Gegenwart von Alkalilauge”. Berichte der Deutschen chemischen Gesellschaft 14 (1): 1459–1461. DOI:10.1002/cber.188101401306.
- ↑ Nielsen, A. T.; Houlihan., W. J. Org. React. 1968, 16, 1-438. (Review)
Literatura
- Heathcock, C. H. (1991). Comp. Org. Syn.. Oxford: Pergamon. str. 133–179. ISBN 0-08-040593-2.






