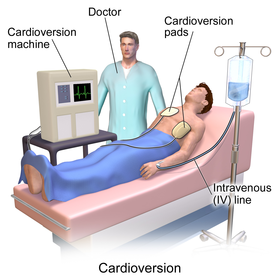
Kardioverzija
| Kardioverzija | |
|---|---|
 | |
| MeSH | D004554 |
[уреди на Википодацима] | |
Kardioverzija označava jednu od invazivnih terapijskih metoda u kardiologiji, koja se često planirano izvodi da bi se uspostavio sinusni ritam kod bolesnika sa perzistentnom tahiaritmijom npr. kod pretkomorske fibrilacije ili u slučajevima kada je aritmija osnovni faktor odgovoran za akutnu srčanu insuficijenciju, hipotenziju, ili pogoršanje angine pektoris kod bolesnika sa koronarnom bolešću. Kardioverzija se može postići lekovima ili električnim šokom. Lekovi su se uobičajeno upotrebljavali sve dok električna kardioverzija nije postala standardna procedura u kardiologiji. Kardioverzija nosi i rizik od tromboembolijskih komplikacija, ukoliko antikoagulantna profilaksa nije započeta pre procedure. Rizik je najveći ako je aritmija trajala duže od 48 sati.[1]
Terminologija
- Kardioverzija medikamentima
- Podrazumeva upotrebu lekova da bi se uspostavio sinusni ritam kod bolesnika sa perzistentnom tahiaritmijom.
- Kardioverzija jednosmernom strujom (енгл. direct-current, DC cardioversion)
- Podrazumeva oslobađanje električnog šoka, koji je vremenski usklađen (sinhronizovan) sa električnom aktivnošću srca, prema R-zupcima u elektrokardiogramu (EKG). Ova tehnika osigurava da do električne stimulacije ne dođe tokom vulnerabilnog perioda srčanog ciklusa, koji obuhvata period od 60 do 80 msec pre, do 20 do 30 msec posle vrha T-talasa.[2]
- Električna kardioverzija
- Onačava termin koji se odnosi na normalizovanje svih poremećenih srčanih ritmova, osim komorske fibrilacije.
- Defibrilacija
- To je termin koji podrazumeva asinhrono električno pražnjenje, koje je podesno za korekciju fibrilacije srčanih komora, ali ne i fibrilacije srčanih pretkomora ili atrijalne fibrilacije.
Istorija
Ocem minijaturnih defibrilatora koji se ugrađuju u telo pacijenta Američki naučnik Majkl Mirovski koji je krajem 1960-ih godina prvi počeo sa razvojem "ugradljivih defibrilatora" nakon što je njegov prijatelj i mentor Hari Heler preminuo od posledica ventrikularne aritmije.
Prvi uspešno primenjen ugradljivi defibrilator napravljen je 1980. godine. Sastojao se od jednostavnog kola koje je okidalo dovoljno velike impulse u slučaju detekttovanja ventrikularne aritmije. Od tada, napravljen je veliki napredak u razvoju defibrilatora, tako da su danas, ugradljivi kardioverter defibrilatori (Implantable Cardioverter Defibrilators skr. ICD) postali najbolja terapija za pacijente sa ventrikularnom tahikardijom.
Metode kardioverzije
Farmakološka kardioverzija
Kardioverzija lekovima uobičajeno se upotrebljavala sve dok nije otkrivena električna kardioverzija. Razvojem novih lekova povećana je popularnost farmakološke kardioverzije, iako kod njihove primene postoje i neke nepogodnosti, kao što su rizik od komorske tahikardije oblika torsades de pointes, ili rizik od drugih ozbiljnijih aritmija.[3]
Farmakološka kardioverzija bila je predmet intenzivnog istraživanja tokom protekle decenije. Iako je farmakološki pristupak jednostavniji, ona je manje uspešan od električne kardioverzije. U odabranim slučajevima farmakološka kardioverzija može biti pokušana i u kućnim uslovima. Osnovni rizik kod farmakološke konverzije je toksičnost antiaritmijskih lekova.[4]
Farmakološka kardioverzija, bez obzira na novootkrivane medikamente, još uvek je manje uspešna od električne kardioverzije, i pored toga što elektrokonverzija zahteva uspavljivanje bolesnika ili njegovu sedaciju, što kod farmakološke konverzije nije potrebno.[5]
Električna kardioverzija

Kardioverzija električnim šokom zasniva se na upotrebi kratkotrajnog električnog šoka preko elektroda postavljenih na grudnom košu bolesnika. Jedna elektroda postavlja se na predeo vrha srca, a druga desno, na gornji deo grudne kosti (stenuma), da bi se primenom električnog šoka jednosmeme struje (DC-direct current) izvršila depolarizacija srčanog mišića (miokarda) i prekinula tahikardija, odnosno tahiaritmija.[6]
Tehnička razmatranja električne kardioverzije
Uspešnost kardioverzije zavisi od prirode osnovnog srčanog oboljenja i gustine struje dostavljene pretkomorskom miokardu. S druge strane, gustine struje dostavljene pretkomorskom miokardu zavisi od voltaže kondenzatora defibrilatora, oblika izlaznog strujnog talasa, veličine i položaja električnih pedala i transtorakalnog otpora.[6]
Sa povećanjem otpora, smanjuje se gustina struje koja dospeva do srčanog mišića pretkomora, pri datoj površini pedala. Transtorakalni otpor zavisi od veličine i sastava električnih pedala, dodirne sredine između elektroda i kože, udaljenosti između pedala, telesne veličine bolesnika, faze respiratornog ciklusa, broja primenjenih šokova i vremenskog perioda između šokova.[6]
Zatao je za uspešnu kardioverziju veoma važno obratiti pažnju na sve ovde navedene činioce.[6]
Klinička razmatranja
Kardioverzija medikamentima

Farmakološka kardioverzija najuspešnija kada se započne tokom sedam dana od početka tahiaritmije (fibrilacije).[7][8][9][10] Većini bolesnika sa patološkom fibrilacijom prva dokumentovana epizoda fibrilacije u vreme lečenja je nepoznat. Veliki procenat bolesnika sa pretkomorskom fibrilacijom skorašnjeg početka dožvi spontanu kardioverziju od 24 časa do 48 časova.[11][12] Spontana konverzija je ređa kod bolesnika sa pretkomorskom fibrilacijom dužeg trajanja (duže od sedam dana) pre početka lečenja, a i uspešnost farmakološke kardioverzije kod bolesnika sa perzistentnom pretkomorskom fibrilacijom je takođe znatno smanjena.
Određeni lekovi imaju odgođen početak delovanja, te je za kardioverziju potrebno nekoliko dana.[13] Prema nekim studijama, farmakološko lečenje skraćuje period do kardioverzije, u poređenju sa placebom (lažnim lekom), ali bez uticaja na procenat bolesnika koji ostaju u sinusnom ritmu nakon 24 časa. Farmakološka terapija ubrzava uspostavljanje sinusnog ritma kod bolesnika sa fibrilacijom skorašnjeg početka, ali je prednost u odnosu na placebo vrlo mala nakon 24 do 48 časova, i znatno je manje uspešna kod bolesnika sa perzistentnom fibrilacijom (neki lekovi su čak i bez efekta).
Kardioverzija električnim šokom

Kardioverzija se izvodi u odgovarajućojj opštoj anesteziji, kako bi se izbegao bol prilikom primene električnog šoka. U anesteziji se prepopručuje primena kratkodelujućih anestetik ili sedativa, jer je potrebno da se posle procedure bolesnik brzo oporavi, jer ova intervencija ne zahteva bolničko lečenje tokom noći.[14] Pre postupka kardioverzije bolesniku ne treba davati obrok.
Električni šok treba da je pravilno sinhronizovan sa QRS kompleksom, što zahteva monitoring R-zupca u odgovarajućem, odabranom odvodu. Osim amplitude R-zupca, važno je da se u datom odvodu dobro vidi P-talas, što olakšava procenu ishoda procedure.
Kod primene monofaznog strujnog talasa, početna energija za konverziju pretkomorskog flatera može biti mala (50 J).
Za konverziju pretrkomorske fibrilacije potrebna je veća energija, od najmanje 200 J.
Energija se tokom kardioverzije sukcesivno povećava za po 100 J, do maksimalnih 400 J. Pojedini lekari počinju sa većim energijama kako bi smanjili broj primenjenih šokova (i ukupno primenjenu energiju). Primenom bifaznog strujnog talasa potrebna je manja energija.
Da bi se izbeglo oštećenje srčanog mišića, vremenski razmak između dva uzastopna šoka ne bi trebalo da bude manji od jednog minuta.[15]
Rizici i komplikacije
Nema jasnih dokaza da se rizik od tromboembolijskih komplikacija i moždanog udara (kao najznačajnijih) razlikuje kod farmakološke i električne metode konverzije. Preporuke za antikoagulantnu terapiju u vreme kardioverzije su iste za obe metode.
Rizici kardioverzije prvenatveno se odnose na embolijska začepljenja krvnih sudova i srčane aritmije, dok su oštećenja srčanog mišića od malog značaja.
- Embolije
Pojava tromboembolija evidentirana je kod 1–7% odsto bolesnika kojima nisu preventivno koristili antikoagulantnu terapiju pre kardioverzije npr. pretkomorske fibrilacije.[16][17]
- Aritmije
Nakon obavljene kardioverzije mogu se javiti različite bezopasne aritmije, najčešće komorske i pretkomorske ekstrasistole, bradikardija i kratki periodi sinusnog zastoja, koje obično spontano prolaze.[18]
Znatno opasnije aritmije (komorska tahikardija i fibrilacija), mogu nastati kod bolesnika sa hipokalijemijom ili intoksikacijom digitalisom.[19][20] Da bi se ovo izbeglo, nivo kalijum u serumu treba da bude u normalnim granicama.
Kontraindikovan je pokušaj kardioverzije u slučajevima intoksikacije digitalisom, zato što se u tom slučaju izazvane komorske tahiaritmije teško mogu zaustaviti. Serumska koncentracija digitalisa u terapijskim granicama ne isključuje mogućnost kliničke toksičnosti, ali uglavnom nije povezana sa malignim komorskim aritmijama tokom kardioverzije,[21] te nije neophodno rutinski obustaviti upotrebu digoksina pre planirane kardioverzije pretkomorske fibrilacije.
Kod bolesnika sa dugotrajnom pretkomorskom fibrilacijom, kardioverzija često otkriva osnovno oboljenje sinusnog čvora. Spor komorski odgovor pri pretkomorskoj fibrilaciji, u odsustvu lekova koji usporavaju sprovođenje kroz AV čvor, može ukazati na osnovni poremećaj atrioventrikularnog sprovođenja. Ovo treba imati u vidu u proceni bolesnika za kardioverzije, kako bi se izbegla simptomatska bradikardija. Ako je očekivani rizik visok, može se profilaktički upotrebiti transkutani ili transvenozni privremeni pejsmejker.[22]
- Oštećenje srčanog mišića
Eksperimenti na životinjama pokazali su da postoji široka granica bezbednosti između energije potrebne za kardioverziju fibrilacije i energije koja dovodi do klinički značajnog oštećenja srčanog mišića[298,299].[23][24] Čak i bez očiglednog oštećenja srčanog mišića, nakon kardioverzije može se na elektrokardiogramu javiti prolazna elevacija ST segmenta,[25] [26] i može doći do porasta serumske koncentracije kreatin-kinaze. Kod 10% bolesnika zabeležen je blagi porast u koncentraciji izoenzima MB kreatinin-kinaze iznad nivoa, za koji se smtra da oštećuje skeletne mišiće, što je korelira sa količinom primenjene energije.[27] U brojnim istraživanjima oštećenje srčanog mišića (miokarda) koje bi se povezalo sa kardioverzijom primenom jednosmerne struje, čak i na mikroskopskom nivou, nije potvrđeno pa samim tim nije klinički značajno.
Prevencija
Pre električne kardioverzije, posebno za svakog bolesnika, treba razmotriti potrebu za profilaktičkom antiaritmijskom terapijom, kako bi se sprečio rani povratak aritmije. Na primer, kod bolesnika sa lone pretkomorskom fibrilacijom relativno kratkog trajanja postoji manja verovatnoća da će se fibrilacija rano vrati, u odnosu na bolesnika sa srčanim oboljenjem i fibrilacijom dužeg trajanja.
Ukoliko se fibrilacija povrati (posebno ako se povrati ubrzo nakon kardioverzije), preporučuje se antiaritmijska terapija pri drugom pokušaju električne kardioverzije.
Naredne kardioverzije imaju ograničenu vrednost, a bolesnike bi trebalo pažljivo odabirati. Na primer, kod bolesnika sa izraženim simptomima, ponavljane kardioverzije (ne suviše često) mogu biti prihvatljiv terapijski pristup.
Izvori
- ^ Josephson, M.E. (2002) Clinical cardiac electrophysiology: Techniques and interpretations. Philadelphia: Lippincott Williams & Wilkins, 3d ed
- ^ Hou, C. J.; Chang-Sing, P.; Flynn, E.; et al. (1995). „Determination of ventricular vulnerable period and ventricular fibrillation threshold by use of T-wave shocks in patients undergoing implantation of cardioverter/defibrillators”. Circulation. 92: 2558—64. .
- ^ „Medikamentozna konverzija atrijalne fibrilacije kinidinom”. www.tmg.org.rs. Приступљено 2022-12-02.
- ^ Grujić M. Srčane aritmije i principi terapije. U: Klinička kardiovaskularna farmakologija. Kažić Z, Ostojić M. Ed. Integra, Beograd, 2004. 387-405
- ^ Ostojić M, Kanjuh V. Medikamenti u primarnoj i sekundarnoj prevenciji. Arh.farm. 2000; (1-2): 27-30.
- ^ а б в г Shea, Julie B.; Maisel, William H. (2002). „Cardioversion”. Circulation. 106 (22): e176—8. PMID 12451016. doi:10.1161/01.CIR.0000040586.24302.B9.
- ^ Borgeat A, Goy JJ, Maendly R, Kaufmann U, Grbic M, Sigwart U (1986). „Flecainide versus quinidine for conversion of atrial fibrillation to sinus rhythm”. American Journal of Cardiology. 58: 496—8. CS1 одржавање: Вишеструка имена: списак аутора (веза).
- ^ Suttorp, M. J.; Kingma, J. H.; Lie AH; Mast, E. G. (1989). „Intravenous flecainide versus verapamil for acute conversion of parox- ysmal atrial fibrillation or flutter to sinus rhythm”. American Journal of Cardiology. 63: 693—6. .
- ^ Suttorp, M. J.; Kingma, J. H.; Jessurun ER; Lie, A. H.; van Hemel NM, Lie KI (1990). „The value of class IC antiarrhythmic drugs for acute conversion of paroxysmal atrial fibrillation or flutter to sinus rhythm”. Journal of the American College of Cardiology. 16: 1722—7. .
- ^ Platia, E. V.; Michelson, E. L.; Porterfield JK; Das, G. (1989). „Esmolol versus verapamil in the acute treatment of atrial fibrillation or atrial flutter”. American Journal of Cardiology. 63: 925—9. .
- ^ Capucci, A.; Lenzi, T.; Boriani, G.; et al. (1992). „Effectiveness of loading oral flecainide for converting recent-onset atrial fibrillation to sinus rhythm in patients without organic heart disease or with only systemic hypertension”. American Journal of Cardiology. 70: 69—72. .
- ^ Capucci A, Boriani G, Rubino I, Della CS, Sanguinetti M, Magnani B (1994). „A controlled study on oral propafenone versus digoxin plus quinidine in converting recent onset atrial fibrillation to sinus rhythm”. Int J Cardiol. 43: 305—13. CS1 одржавање: Вишеструка имена: списак аутора (веза)
- ^ Kochiadakis, G. E.; Igoumenidis, N. E.; Solomou MC; Kaleboubas, M. D.; Chlouverakis GI; Vardas, P. E. (1999). „Efficacy of amiodarone for the termination of persistent atrial fibril- lation”. American Journal of Cardiology. 83: 58—61. .
- ^ Lesser, M. F. (1990). „Safety and efficacy of in-office cardioversion for treatment of supraventricular arrhythmias”. American Journal of Cardiology. 66: 1267—8. .
- ^ Dahl CF, Ewy GA, Warner ED, Thomas ED. Myocardial necrosis from direct current countershock: effect of paddle electrode size and time interval between discharges. Circula- tion. 50 956–61.
- ^ Bjerkelund, C. J.; Orning, O. M. (1969). „The efficacy of anticoagulant therapy in preventing embolism related to DC electrical conversion of atrial fibrillation”. American Journal of Cardiology. 23: 208—16. .
- ^ Arnold, A. Z.; Mick, M. J.; Mazurek RP; Loop, F. D.; Trohman, R. G. (1992). „Role of prophylactic anticoagulation for direct current cardioversion in patients with atrial fibrillation or atrial flutter”. Journal of the American College of Cardiology. 19: 851—5. .
- ^ Rabbino, M. D.; Likoff, W.; Dreifus, L. S. (1964). „Complications and limitations of direct current countershock”. JAMA. 190: 417—20. .
- ^ Lown, B.; Kleiger, R.; Williams, J. (1965). „Cardioversion and digitalis drugs: changed threshold to electric shock in digitalized animals”. Circ Res. 17: 519—31. .
- ^ Aberg, H.; Cullhed, I. (1968). „Direct current countershock complica- tions”. Acta Med Scand. 183: 415—21.
- ^ Ditchey, R. V.; Karliner, J. S. (1981). „Safety of electrical cardioversion in patients without digitalis toxicity”. Annals of Internal Medicine. 95: 676—9. .
- ^ Mancini, G. B.; Goldberger, A. L. (1982). „Cardioversion of atrial fibril- lation: consideration of embolization, anticoagulation, pro- phylactic pacemaker, and long-term success”. American Heart Journal. 104: 617—21. .
- ^ Lipkin, D. P.; Frenneaux, M; Stewart, R.; Joshi, J; Lowe, T.; McKenna, W. J. (1988). „Delayed improvement in exercise capacity after cardioversion of atrial fibrillation to sinus rhythm”. British Heart Journal. 59: 572—7. .
- ^ Patton, J. N.; Allen, J. D.; Pantridge, J. F. (1984). „The effects of shock energy, propranolol, and verapamil on cardiac damage caused by transthoracic countershock”. Circulation. 69: 357—68. .
- ^ Van Gelder IC, Crijns HJ, Van der LA, van Gilst WH, Lie KI (1991). „Incidence and clinical significance of ST segment eleva- tion after electrical cardioversion of atrial fibrillation and atrial flutter”. American Heart Journal. 121: 51—6. CS1 одржавање: Вишеструка имена: списак аутора (веза).
- ^ Ehsani, A.; Ewy, G. A.; Sobel, B. E. (1976). „Effects of electrical counter- shock on serum creatine phosphokinase (CPK) isoenzyme activity”. American Journal of Cardiology. 37: 12—8. .
- ^ Lund M, French JK, Johnson RN, Williams BF, White HD (2000). „Serum troponins T and I after elective cardioversion”. European Heart Journal. 21: 245—53. CS1 одржавање: Вишеструка имена: списак аутора (веза).
Literatura
- Al-Khatib, S. M.; Stevenson, W. G.; Ackerman, M. J.; Bryant, W. J.; Callans, D. J.; Curtis, A. B.; Deal, B. J.; Dickfeld, T.; Field, M. E.; Fonarow, G. C.; Gillis, A. M.; Granger, C. B.; Hammill, S. C.; Hlatky, M. A.; Joglar, J. A.; Kay, G. N.; Matlock, D. D.; Myerburg, R. J.; Page, R. L. (2018). „2017 AHA/ACC/HRS guideline for management of patients with ventricular arrhythmias and the prevention of sudden cardiac death: Executive summary: A Report of the American College of Cardiology/American Heart Association Task Force on Clinical Practice Guidelines and the Heart Rhythm Society”. Heart Rhythm. 15 (10): e190—e252. PMID 29097320. doi:10.1016/j.hrthm.2017.10.035.
- Curtis AB, Tomaselli GF. Approach to the patient with cardiac arrhythmias. In: Libby P, Bonow RO, Mann DL, Tomaselli GF, Bhatt DL, Solomon SD, eds. Braunwald's Heart Disease: A Textbook of Cardiovascular Medicine. 12th ed. Philadelphia, PA: Elsevier; 2022:chap 61.
- Epstein, A. E.; DiMarco, J. P.; Ellenbogen, K. A.; et al. (2013). „2012 ACCF/AHA/HRS focused update incorporated into the ACCF/AHA/HRS 2008 guidelines for device-based therapy of cardiac rhythm abnormalities: a report of the American College of Cardiology Foundation/American Heart Association Task Force on Practice Guidelines and the Heart Rhythm Society”. Journal of the American College of Cardiology. 61 (3): e6—e75. PMID 23265327.
- Minczak BM, Laub GW. Defibrillation and cardioversion. In: Roberts JR, Custalow CB, Thomsen TW, eds. Roberts and Hedges' Clinical Procedures in Emergency Medicine and Acute Care. 7th ed. Philadelphia, PA: Elsevier; 2019:chap 12.
- Myerburg RJ. Approach to cardiac arrest and life-threatening arrhythmias. In: Goldman L, Schafer AI, eds. Goldman-Cecil Medicine. 26th ed. Philadelphia, PA: Elsevier; 2020:chap 57.
- Nattel S, Tomaselli GF. Mechanisms of cardiac arrhythmias. In: Libby P, Bonow RO, Mann DL, Tomaselli GF, Bhatt DL, Solomon SD, eds. Braunwald's Heart Disease: A Textbook of Cardiovascular Medicine. 12th ed. Philadelphia, PA: Elsevier; 2022:chap 62.
- Santucci PA, Wilber DJ. Electrophysiologic interventional procedures and surgery. In: Goldman L, Schafer AI, eds. Goldman-Cecil Medicine. 26th ed. Philadelphia, PA: Elsevier; 2020:chap 60.
Spoljašnje veze
- Cardioversion from the National Institutes of Health
- Pharmacological Cardioversion from the American Academy of Family Physicians Архивирано на сајту Wayback Machine (27. септембар 2011)
- Synchronized Electrical Cardioversion from eMedicine Online
 | Molimo Vas, obratite pažnju na važno upozorenje u vezi sa temama iz oblasti medicine (zdravlja). |










